[프레스나인] 셀리버리는 ‘약리물질 생체 내 전송기술 TSDT’를 이용한 먹는 고도비만 및 제2형 당뇨병 치료신약 CP-SP(Cell-Permeable SOCS3 69-96 Peptide)에 대해 공격적인 임상개발에 돌입한다고 16일 밝혔다.
셀리버리는 이를 위해 CP-SP 펩타이드 신약의 혈뇌장벽(BBB) 투과능 및 비만 치료효능에 대한 신규 미국특허를 출원 완료, 이 펩타이드를 포함하는 구조의 재조합단백질 CP-deltaSOCS3에 대한 유럽연합(EU) 특허등록(9월 17일 거래소 공시)함으로써, 완벽한 지적재산권(IP) 확보와 동시에 임상개발이 본격화되고 있다고 밝혔다.
셀리버리에 따르면 1994년 록펠러대학의 제프리 프리드먼(Jeffrey M. Friedman) 교수에 의해 렙틴(leptin)이 처음 발견된 이후, 비만환자 체내 렙틴 호르몬 양을 조절하면 획기적 고도비만 치료법이 될 것으로 글로벌 제약사들이 기대, 미국 암젠(Amgen) 등이 수차례 임상시험을 진행했지만 모두 실패했다.
고도비만 환자들은 뇌 시상하부에 렙틴 수치가 높음에도 불구하고, 렙틴의 식욕억제신호를 뇌가 인지하지 못해 식욕을 통제하지 못한다. 이 때문에 왕성한 식욕으로 살이 찌는 렙틴저항성(leptin resistance)이 발생, 고도비만 치료가 쉽지 않다는 점이 그간 개발 계획 실패 이유라고 셀리버리는 전했다.
이처럼 렙틴은 글로벌 제약사들이 고도비만 치료제로 개발하기 위해 많은 노력을 기울인 신약개발 타깃이라는 것이다.
이에 뇌 시상하부에서 발생하는 렙틴-렙틴수용체 신호전달체계를 렙틴저항성으로부터 보호하는 신약물을 개발하기 위해선 혈뇌장벽(BBB) 투과를 통해 뇌조직 내 깊숙히 위치하고 있는 시상하부 조직의 뇌신경세포 내부에까지 약물을 전송해야 한다는 게 셀리버리 설명이다.
렙틴-렙틴수용체 결합에 의한 식욕억제 신호전달이 세포 내부에서 제대로 핵 내 유전자 수준에까지 전달될 수 있다고 셀리버리는 덧붙였다.
정상적 신호전달이 이루어져야 식욕을 조절하고 에너지 대사를 촉진시켜 살이 빠지게 하는 비만치료 효과를 나타낼 수 있지만, 이를 가능케 해주는 바이오기술은 현재로선 없는 만큼 그간 신약개발이 어려웠다고 셀리버리 측은 여러 관련 자료들로 설명했다.
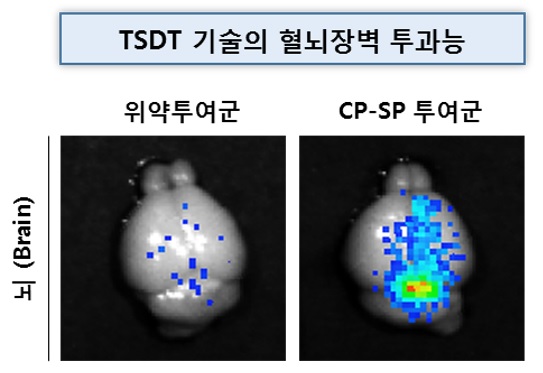
조대웅 셀리버리 대표는 “셀리버리 TSDT 플랫폼기술이 적용된 CP-SP 펩타이드 신약은 혈뇌장벽을 투과해 뇌조직 깊숙히 위치하며 전체 뇌질량의 1/100에 불과한 시상하부 조직에 정확히 전달, 식욕을 억제할 수 있게 한다는 것이 실험적으로 증명했다”고 말했다.
조 대표는 “왜냐하면 CP-SP를 구성하는 aMTD 세포막 투과 펩타이드는 TSDT 플랫폼기술이 제공하는 세포 간 연속 투과성을, 약리물질인 SP 펩타이드는 렙틴-렙틴수용체가 식욕억제신호를 만들어내는 뇌조직·신경세포에만 타겟팅되는 특성을 조합한 융합펩타이드 표적치료제이기 때문”이라고 했다.
이어 그는 “고도비만 질환동물에 CP-SP를 투여한 후 뇌조직 내 CP-SP의 전송 분포를 분석한 결과, CP-SP가 뇌 신경세포 및 성상교세포에 전송될 뿐만 아니라, 시상하부 뇌조직에 식욕조절에 관여하는 신경세포(NPY neuron) 내에도 충분한 양이 전송됐음을 발견했다"고 전했다.
조 대표는 셀리버리의 플랫폼 기술을 활용해 체내에서 식욕억제신호가 식욕을 제어할 수 있도록 할 수 있다고 말했다.
그는 "TSDT 플랫폼기술의 세포 간 연속전송(cell-to-cell transfer) 메커니즘에 의해 혈뇌장벽을 구성하는 혈관 내피세포(endothelial cell) 세포막을 투과한다"며 "이는 계속해서 뇌조직을 구성하는 뇌 신경세포를 연속 투과해 렙틴-렙틴수용체가 존재하는 시상하부 뇌세포 내부에까지 전송 가능해야 렙틴저항성을 극복해 식욕억제신호가 우리몸의 식욕을 제어할 수 있다"고 했다.
셀리버리의 TSDT 플랫폼기술은 이같은 메커니즘을 가능하게 하는 유일한 기술이라고 조 대표는 강조했다.
조 대표는 또한 셀리버리는 최근 미국 뉴저지주의 캡슐 전문제조기업인 캐탈런트(Catalent)사와 CP-SP 캡슐 생산계약을 체결함으로써 먹는 고도비만/제2형당뇨병 치료신약 개발에 본격 나섰다고도 했다.
조 대표는 “임상개발을 위한 경구투여 캡슐치료제로 미국 찰스리버(매사추세츠주)에서 고지방식이에 의한 비만치료 효력시험을 진행하는 동시에 다양한 파이프라인 개발을 통해 호흡을 맞춰온 독성시험 전문 글로벌 위탁연구기관인 미국 코방스(Covance)에서 안전성 평가시험이 진행된다"며 "최종적으로 cGMP 수준의 펩타이드 합성기관인 일본 펩티스타에서 대량생산한 임상시료를 캐탈런트사에서 먹는 캡슐로 만들어 미국에서 조기 임상개발에 돌입한다”고 구체적인 신약개발 계획을 밝혔다.

