[프레스나인] 소화성궤양용제에 쓰이는 ‘니자티딘’ 제제가 또다시 악재를 만났다. 불순물 검출 논란이 가라앉자마자 적응증 삭제라는 변수가 발생한 것이다.
니자티딘 제제의 적응증 삭제가 이뤄질 경우 최근 같은 적응증으로 품목허가를 받은 종근당은 시장 진입이 한층 수월해질 것으로 보인다.
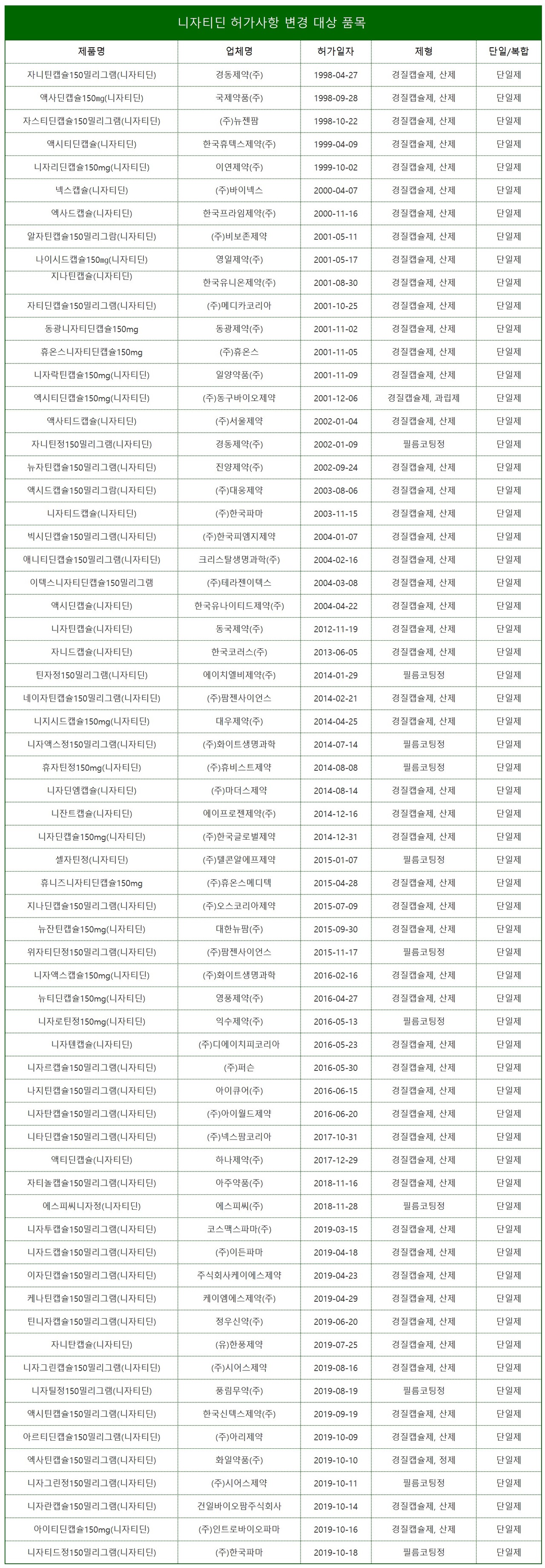
식품의약품안전처는 지난 25일 보건의료단체와 제약사 60곳 등에 니자티딘 단일제(150mg) 허가사항 변경에 대해 의견을 묻는 공문을 발송했다.
현재 니자티딘 적응증은 ▲활동성 위‧십이지장 궤양 치료 및 십이지장 궤양 재발방지 ▲내시경상으로 진단된 미란성 및 궤양성 식도염, 위식도 역류질환(GERD)에 기인한 가슴쓰림(heartburn) 증상 치료 ▲미란‧출혈‧발적‧부종 등 위점막 병변 개선 등으로 규정돼 있다.
식약처는 이중 위점막 병변 개선의 삭제를 추진할 계획이다. 품목 허가 갱신 신청과 관련해 제출된 안전성‧유효성 자료를 검토한 결과, 니자티딘 제제에 대한 허가사항 변경이 필요하다고 판단돼 이같은 변경(안)을 마련했다는 게 식약처 설명이다.
대상 품목은 60개사 65개 제품이다. 해당 제품들은 의약품시장조사기관 아이큐비아 기준 지난해 291억원의 매출을 올렸다. 190억원 실적을 기록한 2020년에 비해 53.2% 성장했다.
니자티딘 제제는 지난 2019년 불순물 검출로 곤욕을 치렀다. 일부 원료의약품 및 완제의약품에서 N-니트로소디메틸아민(NDMA) 잠정관리기준을 미량으로 초과한 것이다. NDMA는 국제보건기구(WHO) 국제 암연구소(IARC)가 지정한 인체발암 추정물질이다.
이에 당시 식약처는 완제의약품 13품목에 대해 잠정적으로 제조 및 판매를 중지하고, 처방을 제한하는 조치를 취했다. 현재도 5개 품목이 판매중지 의약품으로 남아있다.
니자티딘 제제의 위점막 병변 개선 적응증 삭제는 신제품 출시를 앞둔 종근당에겐 반가울만한 소식이다. 종근당은 지난 18일 급성 및 만성위염의 위점막 병변 개선을 적응증으로 하는 ‘지텍(성분명 육계건조엑스)’의 품목허가를 획득했다.
지텍은 녹나무과 육계나무의 줄기 껍질을 말린 약재인 육계에 종근당이 자체 개발한 신규추출법을 적용한 천연물 의약품이다. 종근당은 지난 2013년부터 다양한 생약들을 대상으로 기존 약물 대비 차별화 가능성이 있는 소재와 추출법을 연구하다 육계의 위염 치료 효능을 확인하고 신약 개발에 착수했다.
지텍은 현재 일본을 포함한 다수의 국가와 해외 진출에 대한 협의를 진행 중이다. 국내에는 건강보험 등재 절차와 발매 준비를 마치는 대로 출시할 계획이다.