
13일 정부기관에 따르면 질병관리본부는 올 하반기까지 '유전자검사기관 관리 내실화 가이드라인'을 개발한다. 유전자 검사를 수행하는 기관·기업 운영과 검사 절차, 서비스 제공 위한 법률적으로 요구하는 사항 등을 체계적으로 제시한다.
생명윤리법에서 제시한 유전자검사기관 운영에 필요한 요구사항과 세부 기준이 담긴다. 유전자검사기관 신고 휴·폐업 절차 △동의서 구득과 의뢰 절차 △검사대상물, 검사결과 등 보관·기록절차 △기록보관과 정보 공개 범위 △검사대상물 제공과 폐기 등이다. 유전자 검사기관 목적별 서명동의 방법과 면제절차, 검사 관련 거짓광고와 과대광고 범위도 구체적으로 제시한다.
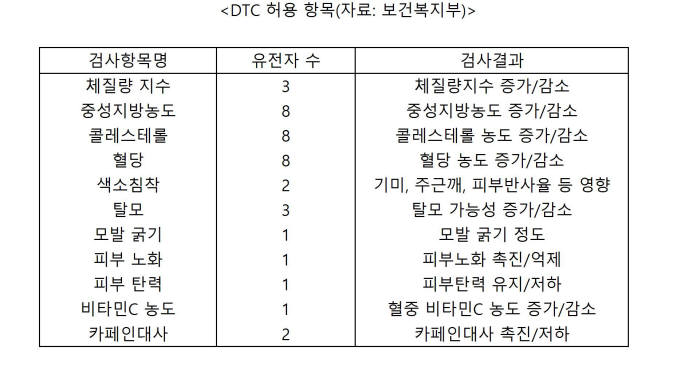
가이드라인은 유전자 검사 수요 증가에 따라 서비스 제공 기관이 늘어나면서 필요성이 제기됐다. 2016년 6월 30일부터 생명윤리법 개정에 따라 의료기관 의뢰 없이 민간 유전자 검사 기업이 직접 수행 가능하다. 혈당, 혈압, 피부노화, 체질량 지수 등 12개 검사항목 46개 유전자 대상이다.
질병관리본부 관계자는 “6개월간 연구, 공청회 등을 거쳐 하반기 가이드라인 개발을 완료한다”면서 “DTC(민간유전자검사) 시장이 열리는 등 수요 확대에 따라 운영 지침을 제시한다”고 말했다.
유전자 검사 업계도 가이드라인 제정에 긍정적이다. DTC 시장 진입과 사업 영위 과정에서 정보가 부족했다. 생명윤리법 등 법률 준수가 중요한 상황에서 가이드라인은 위험요인을 줄인다.
산업계 포괄적 의견 수렴이 관건이다. 업계는 가이드라인이 정보제공, 장기적 위험요인을 줄이는 데 효과적이지만 또 다른 규제나 부담으로 작용할지 우려한다. 정부도 이를 인지, 유전자검사 평가와 관리체계 확립·고도화를 위해 상시 협의체를 만든다. 필요 시 관리 내실화 위한 법령 제·개정, 고시도 마련한다.
유전자 검사업체 관계자는 “DTC 시장 개화 이후 사업을 운영하는 데 정부 지침이 필요하다는 의견이 많았고 실제 정부에 요구했다”면서 “산업계 의견을 충분히 수렴한 상황에서 가이드라인이 만들어지지 않으면 사업에 부담을 주는 규제로 작용할 것”이라고 말했다.
[전자신문 CIOBIZ] 정용철 의료/SW 전문기자 jungyc@etnews.com
저작권자 © PRESS9 무단전재 및 재배포 금지

