[프레스나인] 바이오스플라이스 테라퓨틱스(Biosplice Therapeutics)는 무릎 골관절염 치료신약 후보물질 ‘로어시비빈트(Lorecivivint)’에 대한 임상 3상의 장기 연장시험인 ‘OA-07’ 결과를 지난달 13일 캘리포니아 샌디에고에서 개최된 미국 류마티스학회(ACR)에서 구두 발표했다.
‘로어시비빈트’는 미국 샌디에고 소재 바이오텍인 ‘바이오스플라이스 테라퓨틱스(Biosplice Therapeutics)’가 개발중인 무릎 골관절염 치료신약 후보물질이다. 지난 2021년 3월 삼일제약(000520)이 국내 허가 및 판매에 대한 독점권리를 확보한 바 있다. ‘로어시비빈트’는 ‘CLK/DYRK 키나제(인산화효소)’ 억제제로 ‘Wnt 신호’를 조절하는 기전을 갖고 있어 세계 최초의 골관절염 근본적 치료제(DMOAD ; Disease-Modifying Osteoarthritis Drug)를 목표로 개발되고 있다.
‘OA-07’은 미국에서 12개월 동안 임상 3상인 ‘OA-11’을 완료한 환자중 276명을 대상으로 진행한 장기 연장시험으로 ‘로어시비빈트’를 매년 1회씩 3년간 투여했을 때 ‘구조 개선 가능성(structure improvement potential)’을 평가하고자 설계됐다. ‘OA-07’ 시험 1년차(OA-11 시험 포함 시 2년차) 시험군에는 ‘로어시비빈트’ 0.07mg을 투여했으며, 대조군은 위약을 투여했다. 또한 ‘OA-07 시험’ 2년차(OA-11 시험 포함 시 3년차)에는 시험군 및 대조군 모두 ‘로어시비빈트’ 투여로 전환 해 전체 환자 모두에게 오픈라벨로 ‘로어시비빈트’ 0.07mg를 투여했다. ‘OA-07’ 시험이 진행되는 동안 이전 시험인 ‘OA-11’ 투약 결과에 대해서는 이중맹검을 유지했다.
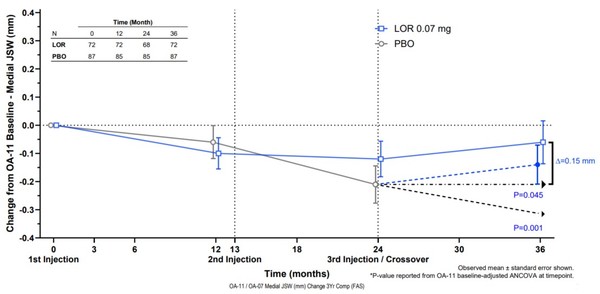
임상 결과 3년간 매년 1회씩 총 3회 ‘로어시비빈트’ 0.07mg을 투약 받은 시험군의 ‘mJSW(36개월)’은 -0.06mm, 위약 대조군의 ‘mJSW(24개월)’은 -0.21mm를 보였다. 두 환자군에서 0.15mm의 유의미한 ‘mJSW’ 차이를 보였으며(p=0.045), 대조군에게 위약을 지속투여(36개월) 했다고 가정한 경우에는 시험군과 위약 대조군의 ‘mJSW’ 차이는 0.26mm로 임상적 및 통계적으로 유의한 결과를 확인했다(p=0.001).
임상 시험에 사용된 ‘mJSW’는 무릎 관절 내측 공간 폭을 의미하며, 해당 너비에 따라 무릎 골관절염 진행 정도를 판단한다. X-레이로 촬영해 측정하며, ‘mJSW’가 작을수록 골관절염 진행이 심한 것으로 판단하며, ‘mJSW’가 증가할수록 골관절염이 개선된 것으로 판단한다.
이번 임상에서 ‘로어시비빈트’는 무릎 골관절염이 상대적으로 덜 심각한 ‘KL 2단계(KL grade 2)’ 환자에서 이점이 더 큰 것으로 확인됐다. 기준선 대비 시험군(36개월)의 ‘mJSW’는 0.17mm의 증가를 보였으며, ‘로어시비빈트’ 투여군으로 전환하기 전 위약 대조군의 마지막 측정 시점(24개월) 대비 통계적으로 유의한 증가가 있었다(p=0.012). 위약 대조군을 ‘로어시비빈트’ 투여군으로 전환하지 않고 계속해서 위약을 36개월간 지속 투여했다고 가정한 경우에는 시험군 과 위약 대조군의 ‘mJSW’ 0.35mm 차이를 보여 임상적 및 통계적으로 유의한 결과를 확인했다(p=0.003).
이번 3상 임상 결과를 발표한 ‘바이오스플라이스’의 ‘유수프 야즈즈(Yusuf Yazici)’ 박사는 “이번 임상결과는 ‘로어시비빈트’의 반복주사가 구조적 변화와 증상적 이점을 모두 제공할 수 있다는 가능성을 의미한다”며 “무릎 골관절염 치료 옵션으로 로어시비빈트를 계속 연구하게 되어 기쁘다”고 밝혔다.
삼일제약 관계자는 “이번 임상결과로 장기 안전성과 유효성이 확인됐다는데 큰 의미가 있다. 무릎 골관절염 치료의 First-in-class 약물로 승인이 기대되는 만큼 국내 독점권리를 보유하고 있는 삼일제약에 의미 있는 신약 포트폴리오가 될 것으로 기대한다”고 밝혔다.