미국·일본 등은 필수적 시스템으로 제도화…의료계, 수가적용 한목소리
[프레스나인] "10년 뒤 6조6500억원에 육박하는 전세계 폐쇄형약물전달장치(Closed system Drug-Transfer Device, CSTD) 시장에서 10%를 점유하겠습니다."

박정건 STS바이오 대표이사는 본지와 만난 자리에서 "국내에서 최초이자 글로벌에서 가장 혁신적"이라며 자사의 CSTD 제품을 소개했다.
CSTD는 환자와 의료종사자의 안전을 항암제 등 유해약물의 노출을 비롯해 약물 내 오염물질 유입을 원천 차단하는 의료기기다. 쉽게 말해, 주사기, 바이알, 수액백(병)에 바늘 대신 연결해 조제(약액 이동), 투약, 폐기 등 모든 단계에서 완벽한 폐쇄 상태를 유지하는 장치를 말한다.
박정건 대표는 병원 및 헬스케어 분야에서 20여년 현장 경험을 닦으며 의료종사자 위해 환경 개선의 필요성을 절감한 것이 창업의 계기가 됐다. 2019년 설립한 STS바이오의 영문 풀네임을 '안전을 지원하는(Supporting the Safety)'이라고 지은 것처럼 사업성과 공익성, 둘다 잡겠다는 야심이 넘쳤다.
박 대표는 첫 아이템으로 CSTD를 주목했다. CSTD는 국내에서는 생소하지만, 미국과 일본 등 의약품 선진국에선 이미 필수적인 시스템으로 제도화된 지 오래다. 미국은 1998년부터 이미 CSTD를 사용했다. 미국약전(USP800)을 통해 CSTD 사용을 의무화하고 있다. 일본은 2012년부터 CSTD를 건강보험 수가로 적용했으며, 대만은 2013년부터 CSTD를 사용하고 있다.
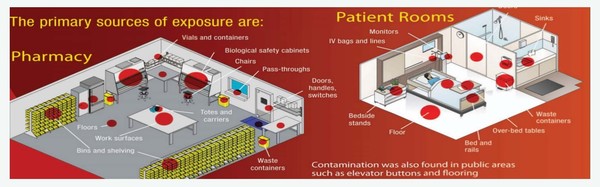
박정건 대표는 "항암제 등 유해약물은 휘발성과 독성이 강해 조제 및 취급 과정에서 건강상 위해 위험을 수반한다"며 "실내 전파를 통해 공기 중 비말 흡입하거나 표면오염으로 피부 침투 우려가 크다"고 말했다.
유해약물은 116종 항암제가 대표적이며, 최기형성(태아 기형), 생식독성, 발암성, 발달독성, 장기독성, 유전자독성을 일으킬 수 있다. 101종은 항바이러스제, 항호르몬제, 바이오의약품 등이 포함된다. 환자를 살리는 항암제가 의료종사자에게는 오히려 독이 될 수 있다는 경고다.
하지만 개발과 상용화 과정은 녹록지 않았다. 글로벌사 등 해외기업이 수십개 CSTD 특허 허들을 깔아놨기 때문이다. 박 대표는 시행착오를 겪으면서 외산제품보다 진보적이자 사용자 편의성까지 우수한 CSTD의 국산화에 마침내 성공했다.
그는 "STS바이오의 CSTD는 항암제뿐만 아니라 프리필드 실린지, 프로포폴, 항생제, 마이크로카테터 결합, 보툴리눔톡신, 피부주사제 등 누출과 오염을 막는 성능이 요구되는 분야에서 다양하게 적용될 수 있도록 호환성이 무궁무진하다"며 "최소잔류랑, 조제효율, 수액병 안전장치, 조제시간, 금속 없음 등 경쟁사 대비 장점이 많은 데다가 가격 경쟁에서도 유리하다"고 설명했다.
STS바이오의 CSTD가 등장하자 의료진에서도 큰 관심을 보였다. 지난해 4월 판매허가를 받은 이후 주요 대학병원들에게 납품을 하기 시작했다. 국내에서도 점차적으로 고객사가 늘어가고 있지만, 오히려 수요가 터진 곳은 STS바이오의 남다른 기술력을 알아본 해외였다.
박 대표는 "우즈베키스탄에 20만불 수출 계약을 체결했으며, 몽골 보건국과 구매의향서를 받았다"며 "CSTD 시장이 열려 있는 일본은 파트너와 비밀유지계약을 체결했다. 2025년 1분기 후생성 의료기기 허가와 같은 해 3분기 일본 공장 설립을 목표로 협의를 이어가고 있다"고 피력했다. 아울러 "세계 최대 시장인 미국을 겨냥해 FDA 신청을 완료했고, CIS 국가 등록은 이미 완료했다"고 부연했다.
다소 늦은 감이 있지만 국내에서도 CSTD의 필요성에 대해서 공감하는 분위기가 형성되며 비로소 제도적 기반을 갖추기 시작하는 모습이다.
박정건 대표는 "식약처에서 CSTD 분류를 2023년 4월 신설했으며, 학회에서도 조제 가이드라인이 나왔다"며 "중대재해처벌법과 태아산재법이 시행되면서 CSTD에 대한 사회적 요구가 높아지고 있다"고 강조했다.
CSTD에 대한 수가가 발목을 잡고 있다는 게 나아가야 할 과제다. CSTD는 급여도 비급여도 아닌 보험 산정불가이기 때문에 대학병원들은 자체 비용으로 구입하고 있는 현실이다. 항암제 조제 무균 행위수가를 높여주면 의료종사자가 좀더 안전한 환경에서 항암제를 조제할 수 있다는 게 의료계의 목소리다. 건강보험심사평가원은 지난해 6월 신청된 CSTD를 포함한 항암제 조제 무균 행위 인상에 대한 조정을 최근 심의 완료해 최종 결과를 기다리고 있는 의료계의 기대감이 어느 때보다 커지고 있다.
박 대표는 "CSTD가 급여로 적용되면 국내에서 적어도 1000억원대 시장이 열릴 것으로 본다"며 "2027년까지 내수로만 600억~700억원 매출을 충분히 달성할 것"이라고 자신했다.
STS바이오는 국내와 해외에서 수요가 크게 늘어날 것을 대비해 신사업과 제조시설 확장을 위한 시리즈A 투자를 유치하고 있다. 이미 일부 SI(전략적 투자자)가 낙점됐으며, 거물급 투자자가 눈독을 들이고 있다는 후문이다.
마지막으로 박정건 대표는 "STS바이오는 자사의 CSTD가 가장 진보적이고 가격 이점이 있기 때문에 글로벌에서도 충분히 경쟁력이 있다"며 "장기적으로 전세계 CSTD 시장의 10%를 점유하겠다는 목표"라고 덧붙였다.


