FDA와 임상프로토콜 등 조율…치료목적사용신청 계획
[프레스나인] 셀리버리는 미국 식품의약국(FDA)와 항바이러스·항염증 코로나19 면역치료제 'iCP-NI'의 임상 1상 후 2상 진행 또는 임상1·2상 동시 진행 등 임상프로토콜 작성, 환자모집, 용량설정, 병상확보 및 치료목적사용신청 (EAP) 계획 등을 조율하고 있다고 23일 밝혔다.
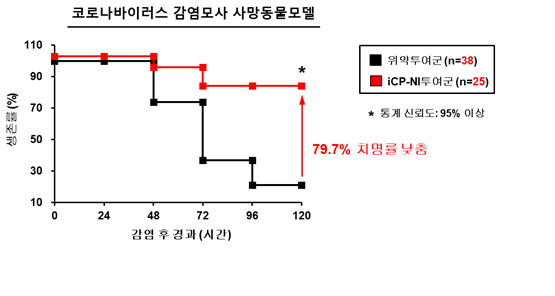
iCP-NI는 바이러스 감염으로 인해 죽음에 이르는 소동물 및 영장류 코로나19 사망모델에서 치명률을 낮추는 치료효능을 확인했다.
조대웅 대표는 "iCP-NI는 중증염증을 제어해 패혈증으로 인한 조직파괴, 혈전생성, 다발성 장기부전 등을 억제하고 생명을 보존할 수 있게 디자인된 항염증 치명률 제어 면역치료제"라고 밝혔다.
iCP-NI는 내재면역시스템 통제를 통해 현재까지 수천마리(6000수 이상) 수준의 개체에서 치명률을 제어할 수 있다.
미국에서 진행된 지금까지의 치료효능 평가결과를 종합하면, iCP-NI는 바이러스의 종류 및 증식, 복제기전, 변이성에 상관없이 코로나19 조기치료 및 사망에 이르는 치명률 감소효능을 증명했다.
조 대표는 "죽음에 이를 수 있는 중증환자들에 대해서는 아예 효능이 없거나 치명률을 낮추지 못한다는 세계보건기구 (WHO)의 공식발표 등으로 인해, 치명률을 제어할 수 있는 코로나19 면역치료제 iCP-NI의 개발이 더욱 중요해 졌다"고 강조했다.
Tag
#셀리버리
저작권자 © PRESS9 무단전재 및 재배포 금지

